3.7. Change of Phase
물은 지구 표면 근처에서 겪는 온도와 압력에서 물질의 한 상태(고체, 액체, 기체)에서 다른 상태로 변화합니다. 흥미롭게도, 물은 지구 상에서 물방울, (구름처럼 보이는) 얼음 결정, 그리고 수증기와 같이 이 세 가지 단계 모두에서 자연적으로 존재하는 유일한 물질입니다.
물은 강력한 열전달 방법으로 만드는 몇몇 독특한 열 특성을 가지고 있습니다. 자연 발생 물질 중 열용량이 가장 높습니다.
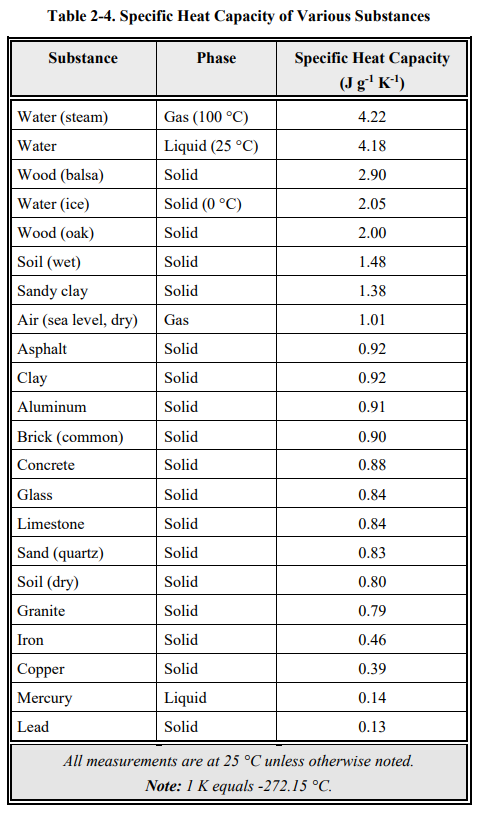
물이 다른 물질보다 열에너지를 흡수하는 용량이 훨씬 크다는 것을 의미합니다. (결과적으로 온도 변화가 거의 없습니다.) 이러한 특성들은 물을 이상적인 열전달 메커니즘으로 만들고 날씨와 기후에 중요한 영향을 미칩니다.
3.7.1. Latent Heat
잠열은 어떤 물질이 상태 변화를 겪을 때 단위 질량에 의해 방출되거나 흡수되는 열 에너지의 양입니다. 단위는 일반적으로 그램 당 줄(J/g)로 표현됩니다. 아래 [Firgure 3-4]는 물이 상태 변화를 겪을 때 발생하는 잠열 과정을 보여줍니다.
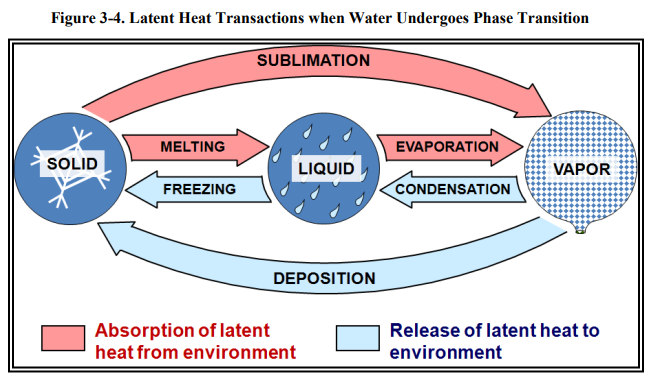
물의 상태 변화하는 동안 물과 물 주위 환경 사이에서 열이 교환됩니다. 상태 변화를 하고 있는 동안 물 주변 환경의 온도가 바뀔지라도, 상태 변화를 하고 있는 물의 온도는 상태 변화가 끝날 때까지 일정하게 유지됩니다. 즉, 잠열(사용 가능한 열)은 오로지 물의 상태를 변화시키는 데만 관여하며, 온도를 변화시키는 데에는 관여하지 않는다는 것입니다. 물의 상태 변화에는 6개의 변화가 있는데, 그중 3개는 물 주변 환경으로부터 잠열 흡수(승화, 융해, 기화), 나머지 3개는 물 주변 환경에 대해 열 에너지 방출(승화, 액화, 응고)과 관련이 있습니다.
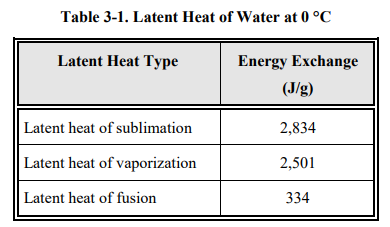
융해는 고체가 액체로 변하는 과정입니다. 융해 과정 동안, 물은 융해열 때문에 334(J/g)의 열을 흡수합니다. 반대로, 응고는 334(J/g)의 열을 밖으로 방출합니다.
기화는 액체가 기체로 변화는 과정입니다. 기화 과정 동안, 물은 증발 잠열에 의해 2,501(J/g)의 열을 흡수합니다. 반대 과정인 액화는 주변으로 2,501(J/g)의 열을 방출합니다.
승화는 고체가 기체로 변하는 과정입니다. 승화 과정 동안, 물은 주변으로부터 2,834(J/g)의 승화열을 흡수합니다. 반대 과정도 승화라고 부르며 주변으로부터 2,834(J/g)의 열을 방출합니다.
잠열 교환과 관련된 에너지의 양을 과소평가해서는 안됩니다. 수증기가 구름과 비로 응축되면서 하루 평균 5,200만 줄(52 million trillion joules per day)의 허리케인을 방출합니다. 이 수치는 2005년 전 세계 에너지 소비량의 약 40배에 해당합니다.
- 열용량(heat capacity) : 어떤 물질의 온도를 1℃ 또는 1K 높이는데 필요한 열량입니다.
- 열량(quantity of heat) : 열량은 물체가 주거나 받는 열의 양, 즉 열에너지의 양입니다.
- 비열 용량(specific heat capacity) : 어떤 물질 1g의 온도를 1℃만큼 올리는 데 필요한 열량을 말합니다.
- 열에너지(heat energy) : 열의 형태를 취한 에너지. 물체의 온도를 변화시키거나 상태변화를 일으키는 에너지를 말합니다.
- 잠열(latent heat) : 물질이 온도·압력의 변화를 보이지 않고 평형을 유지하면서 한 상태에서 다른 상태로 전이할 때 흡수 또는 발생하는 열입니다.
- 물질의 상태변화 종류 : 융해(고체→액체), 기화(액체→기체), 액화(기체→액체), 응고(액체→고체), 승화(고체↔기체)
※ U.S. Department of Transportation Federal Aviation Administration, FAA Advisory Circular (AC) 00-6B, AVIATION WEATHER, page 3-5~7 해석